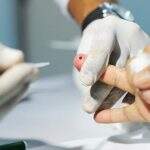
Normas para notificação de lotes-piloto de medicamentos são alteradas pela Anvisa
Decisão colegiada RDC 4/2015 do órgão dispõe uma simplificação do procedimento
Arquivo –
Notícias mais buscadas agora. Saiba mais
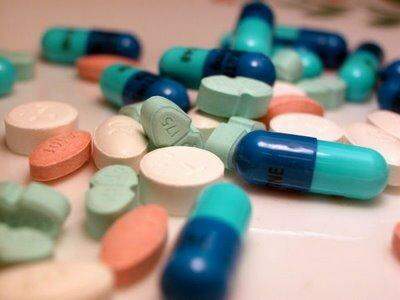
Decisão colegiada RDC 4/2015 do órgão dispõe uma simplificação do procedimento
Publicado no Diário Oficial da União desta quinta-feira (29) uma resolução da Agência Nacional de Vigilância Sanitária (Anvisa) determina uma mudança para o processo de notificação dos lote-piloto de medicamentos.
De acordo com a decisão da Diretoria Colegiada do órgão, RDC 4/2015, os fabricantes nacionais agora estão dispensados de ter que enviar notificações da produção destes lotes ao órgão.
Para efeitos de controle sanitário da produção destes lotes-piloto, a empresa deverá manter registrada documentação, além da responsabilidade de arquivamento da documentação durante toda a validade do registro.
O intuito da medida é reduzir a quantidade de petições-notificações referentes a lotes-piloto. Só entre 2010 e 2014 a Anvisa registrou o encaminhamento de 17.041 processos desse gênero, com uma média anual de 4016 documentos para arquivamento no órgão.
A Anvisa tem trabalhado em prol do aprimoramento do seu estoque regulatório, por meio de medidas de de simplificação, desburocratização e melhoria do acesso aos atos normativos.
Notícias mais lidas agora
- Carreta atropela mulher em bicicleta elétrica na Rua da Divisão
- Papai Noel dos Correios: a três dias para o fim da campanha, 3 mil cartinhas ainda aguardam adoção
- VÍDEO: Motorista armado ‘parte para cima’ de motoentregador durante briga no trânsito de Campo Grande
- VÍDEO: Menino fica ‘preso’ em máquina de pelúcia durante brincadeira em MS
Últimas Notícias
Com entrada gratuita, Academia Sul-Mato-Grossense de Letras promove cantata natalina com 6 corais da capital
Cantata Natalina acontece nesta sexta-feira, dia 13 de dezembro
Conselheira de Batayporã fica ferida após veículo oficial se envolver em acidente na MS-134
As informações apontam que o carro oficial foi fechado por uma carreta
Dono de espetinho preso por vender carne em meio a baratas e moscas é solto com fiança de R$ 1,4 mil
Durante interrogatório, empresário confessou que usava sal de pecuária – sal mineral usado para gado – para salgar os espetinhos
Contrato de ampliação de Hospital Municipal de Aparecida do Taboado tem aditivo e valor vai para R$ 1,2 milhão
Houve um reflexo financeiro positivo no contrato devendo ser empenhado o valor de R$ 182.508,91
Newsletter
Inscreva-se e receba em primeira mão os principais conteúdos do Brasil e do mundo.