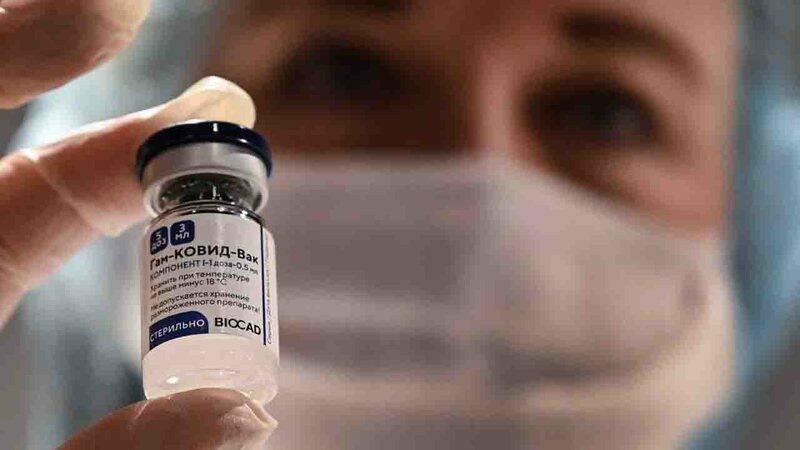
A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou com condicionantes e limitação de doses, pedido feito por Estados e pelo Ministério da Saúde para a importação das vacinas contra covid-19 Sputnik V, da Rússia, e Covaxin, da Índia, nesta sexta-feira (04).
As doses importadas serão limitadas ao equivalente de 1% da população de cada Estado que apresentou o pedido de importação, no caso da Sputnik V, e 1% da população do País no caso da Covaxin.
“Entendemos que essa vacina não deverá ser utilizada por pessoas com hipersensibilidade a qualquer um dos componentes da fórmula, grávidas, lactantes, menores de 18, mulheres em idade fértil que querem engravidar, enfermidades graves ou não controladas e antecedentes de anafilaxia”, disse o gerente-geral de medicamentos da Anvisa, Gustavo Mendes.
Também não poderão receber a vacina, quem tenha recebido outra vacina contra covid-19, hepatite B ou C. Tenham recebido imunoglobulinas ou hemoderivados 3 meses antes, tenham recebido tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação 36 meses, tenham recebido terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos, disse o gerente da Anvisa.
A limitação das doses será usado como estudo clínico e os governos terão que fazer um acompanhamento de eficácia, segurança, e eventuais eventos adversos do imunizante. Tudo será pela acompanhado pela Anvisa para avaliar uma ampliação da importação das duas vacinas.
O repasse de recursos, entretanto, só pode ser feito após autorização da Anvisa para entrada da vacina em território brasileiro. Outra opção seria o STF (Supremo Tribunal Federal) decidir em favor dos estados pela aquisição. Mas, o Supremo deu prazo para a agência reguladora deliberar sobre o assunto.
Segundo dados publicados na revista científica “The Lancet”, a eficácia da Sputnik V após aplicação das duas doses é de 91,6%.